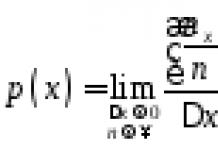Существуют различные методы определения концентрации (точнее активности) ионов водорода (и, соответственно, концентрации гидроксид-ионов). Один из простейших (колориметрический) основан на использовании кислотно-основных индикаторов. В качестве таких индикаторов могут служить многие органические кислоты и основания, которые изменяют свою окраску в некотором узком интервале значений рН.
Индикаторы представляют собой слабые кислоты или основания, которые в недиссоциированной и в диссоциированной (ионной) формах имеют разную окраску.
Пример.
1.Фенолфталеин представляет собой кислоту, которая в молекулярной форме (HJnd) при рН8,1 бесцветна. Анионы фенолфталеина (Jnd -) при рН9,6 имеют красно-фиолетовую окраску:
H Jnd H + + Jnd -
Бесцветный красно-фиолетовый
рН8,1 рН9,6
При уменьшении концентрации ионов Н + и увеличении концентрации ионовOH - молекулярная форма фенолфталеина переходит в анионную из-за отрыва от молекул иона водорода и связывания его с гидроксид-ионом в воду. Поэтому при рН9,6 раствор в присутствии фенолфталеина приобретает красно-фиолетовую окраску. Наоборот, в кислотных растворах при рН8,1 равновесие смещается в сторону молекулярной формы индикатора, не имеющей окраски.
2.Метиловый оранжевый представляет собой слабое основание JndOH, которое в молекулярной форме при рН 4,4 имеет желтый цвет. Катионы Jnd + при рН3,0 окрашивают раствор в красный цвет:
JndOH Jnd + + OH -
желтый красный
рН4,4 рН3,0
Кислотной формой индикатора называют форму, которая преобладает в кислотных растворах, а основной формой – ту, которая существует в основных (щелочных) растворах. В некотором промежутке значений рН в растворе может одновременно находиться в равновесии некоторое количество обеих форм индикатора, вследствие чего возникает переходная окраска индикатора, - это интервал рН перехода окраски индикатора, или просто интервал перехода индикатора.
В табл.1 показаны интервалы перехода некоторых часто используемых индикаторов.
Таблица 1
Кислотно-основные индикаторы
|
Индикатор |
Значение рН |
|||||||||||||
|
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 |
||||||||||||||
|
Тимоловый синий | ||||||||||||||
|
Метиловый оранжевый |
желто-оранжевая |
|||||||||||||
|
Бромфеноловый синий | ||||||||||||||
|
Ализариновый красный |
фиолетовая |
|||||||||||||
|
Метиловый красный | ||||||||||||||
|
Феноловый красный | ||||||||||||||
|
Фенолфталеин |
бесцветная |
красная (розовая) |
||||||||||||
|
Ализариновый желтый |
бледно-желтая |
желто-коричн-евая |
||||||||||||
|
Индиго карминовый |
11,6-14,0 14- желтая |
|||||||||||||
Для быстрого определения рН удобно также пользоваться раствором универсального индикатора, представляющего собой смесь различных индикаторов и имеющего большой интервал перехода (значения рН от 1 до 10). На основе универсального индикатора промышленностью выпускаются специальные бумажные ленты для определения рН у растворов путем сравнения со специальной шкалой изменения их окраски под действием испытуемого раствора.
В колориметрическом методе для точного определения рН применяются стандартные буферные растворы, значение водородного показателя которых точно известно и постоянно.
Буферными растворами называются смеси слабых кислот или оснований с их солями. Такие смеси сохраняют определенное значение рН как при разбавлении, так и при прибавлении небольших количеств сильных кислот или щелочей.
В химии есть вещества, обладающие способностью менять свою окраску в присутствии кислот и щелочей. Эти вещества называются индикаторами и применяются для определения реакционной среды. Среда может быть кислой, щелочной и нейтральной.
Этими веществами пропитывают фильтровальную бумагу. Существует много видов различных индикаторных бумаг (из школы все знают словосочетание « лакмусовая бумажка » ), точнее индикаторов, которыми пропитывают бумагу (лакмус , фенолфталеин , метиловый оранжевый и т.д.). Также к индикаторам можно отнести сок красной капусты, вишни и черноплодной рябины. Бумагу пропитывают раствором смеси индикаторов и, поэтому, она окрашивается в разные цвета в разных средах. Для определения кислотности или щелочности среды можно пользоваться бумажкой, пропитанной раствором любого индикатора.
В азотной кислоте бумажка изменила свой цвет на тёмно-красный. Существуют другие кислоты, в которых бумажка меняет свой цвет на красный. Это серная кислота , соляная и др. Эти кислоты называются сильными кислотами. А такие кислоты, как уксусная , лимонная , винная и др., относящиеся, главным образом, к большому классу химических веществ - органических, называются слабыми. В таких кислотах бумажка приобретает розовый цвет.
Значит, с помощью индикаторной бумажки можно определить сильную и слабую кислоту, если они имеют раствор примерно одинаковой концентрации.
В растворе щёлочи бумажка меняет свой цвет на синий. При работе со щелочами соблюдайте осторожность. Не случайно они названы едкими (едкий натр, едкий(-ое) калий(-и)). К щелочам также относятся известковая вода и нашатырный спирт , который неправильно назван « спиртом » . Это его бытовое название. Правильно это вещество называется гидроксид аммония.
От щелочей нужно оберегать глаза и руки, они портят краску, оставляют на столе несмываемые пятна.
Кислотность и щелочность растворов выражают через концентрацию ионов Н + . Для удобства оценки в химию введено выражение рН (читается « пэ-аш » ). рН называется водородным показателем. Это понятие ввёл датский химик Сёренсен в 1909 году: буква « р » - начальная буква датского слова potenz – математическая степень, буква « Н » - символ водорода.
В нейтральном растворе при 25 ° С рН = 7. В кислых растворах рН < 7, и тем меньше, чем кислее раствор; в щелочных растворах рН > 7, и тем больше, чем больше щёлочность раствора; другими словами – чем меньше рН, тем больше концентрация ионов Н + , т. е. выше кислотность среды, и наоборот, чем больше рН, тем меньше концентрация ионов Н + , т. е. выше щёлочность среды.
Так, например, у желудочного сока рН 1, 7 (сильнокислая реакция), у дождевой воды рН 6 (слабокислая), у водопроводной воды рН 7, 5 (слабощелочная), у крови рН 7, 4 (слабощелочная), у слюны рН 6, 9 (слабокислая), у слёз и дистиллированной воды рН 7 (нейтральная).
Универсальной индикаторной бумагой пользуются только для приближённого определения значений рН в широких пределах с точностью около одной единицы рН.
Смотрите также « Как проверить рыбу и мясо на свежесть с помощью индикаторной бумаги ».
Среди многообразия органических веществ встречаются особые соединения, которым характерны изменения окраски в различной среде. До появления современных электронных pH-метров индикаторы были незаменимыми «инструментами» для определения кислотно-основных показателей среды, и продолжают использоваться в лабораторной практике в качестве вспомогательных веществ в аналитической химии, а также при отсутствии необходимого оборудования.
Для чего нужны индикаторы?
Изначально свойство данных соединений изменять цвет в различной среде широко применялось для визуального определения кислотно-основных свойств веществ в растворе, что помогало определить не только характер среды, но и сделать вывод об образующихся продуктах реакции. Растворы индикаторов продолжают использоваться в лабораторной практике для определения концентрации веществ методом титрования и позволяют научиться использовать подручные способы за неимением современных pH-метров.
Существует несколько десятков подобного рода веществ, каждый из которых чувствителен к довольно узкой области: обычно она не превышает 3 пунктов по шкале информативности. Благодаря такому многообразию хромофоров и их малой активности между собой ученым удалось создать универсальные индикаторы, широко применяемые в лабораторных и производственных условиях.
Наиболее используемые индикаторы pH
Примечательно, что помимо идентификационного свойства, данные соединения обладают хорошей красящей способностью, что позволяет использовать их для покраски тканей в текстильной промышленности. Из большого числа индикаторов цвета в химии самыми известными и используемыми являются метиловый оранжевый (метилоранж) и фенолфталеин. Большинство других хромофоров в настоящее время используются в смеси друг с другом, либо для специфических синтезов и реакции.

Метиловый оранжевый
Многие красители получили название благодаря своим основным цветам в нейтральной среде, что присуще и этому хромофору. Метиловый оранжевый является азокрасителем, имеющим группировку - N = N ‒ в своем составе, которая отвечает за переход цвета индикатора в красный в и в желтый - в щелочной. Сами азосоединения не являются сильными основаниями, однако присутствие электродонорных групп (‒ OH, ‒ NH 2 , ‒ NH (CH 3), ‒ N (CH 3) 2 и др.) увеличивает основность одного из атомов азота, который становится способен присоединять протоны водорода по донорно-акцепторному принципу. Поэтому при изменении концентраций ионов H + в растворе можно наблюдать изменение окраски кислотно-основного индикатора.

Подробнее о получении метилового оранжевого
Получают метиловый оранжевый в реакции с диазотирования сульфаниловой кислоты C 6 H 4 (SO 3 H)NH 2 с последующим сочетанием с диметиланилином C 6 H 5 N(CH 3) 2 . Сульфаниловую кислоту растворяют в растворе натриевой щелочи, добавляя нитрит натрия NaNO 2 , а затем охлаждают льдом для проведения синтеза в максимально близких к 0°C температурах и приливают соляную кислоту HCl. Далее готовят отдельный раствор диметиланилина в HCl, который охлажденным вливают в первый раствор, получая краситель. Его дополнительно подщелачивают, и из раствора выпадают в осадок темно-оранжевые кристаллы, которые по истечении нескольких часов отфильтровывают и сушат на водяной бане.
Фенолфталеин
Свое название данный хромофор получил из сложения наименований двух реагентов, которые участвуют при его синтезе. Цвет индикатора примечателен изменением своей окраски в щелочной среде с приобретением малинового (красно-фиолетового, малиново-красного) оттенка, который обесцвечивается при сильном щелочении раствора. Фенолфталеин может принимать несколько форм в зависимости от показателей pH среды, причем в сильнокислых средах он имеет оранжевую окраску.

Этот хромофор получают путем конденсации фенола и фталиевого ангидрида в присутствии хлорида цинка ZnCl 2 или концентрированной серной кислоты H 2 SO 4 . В твердом состоянии молекулы фенолфталеина являются бесцветными кристаллами.
Ранее фенолфталеин активно использовали при создании слабительных веществ, однако постепенно его применение значительно сократилось в связи с установленными кумулятивными свойствами.
Лакмус
Этот индикатор стал одним из первых реактивов, используемых на твердых носителях. Лакмус является сложной смесью природных соединений, которую получают из некоторых видов лишайников. Его используют не только как но и как средство для определения pH среды. Это один из первых индикаторов, который начал использоваться человеком в химической практике: его применяют в виде водных растворов или пропитанных им полосок фильтровальной бумаги. Лакмус в твердом состоянии является темным порошком со слабым аммиачным запахом. При растворении в чистой воде цвет индикатора принимает фиолетовое окрашивание, а при подкислении дает красный цвет. В щелочной среде лакмус переходит в синий, что позволяет использовать его как универсальный индикатор для общего определения показателя среды.

Точно установить механизм и характер реакции, протекающих при изменении pH в структурах компонентов лакмуса не представляется возможным, так как в него может входить до 15 различных соединений, причем некоторые из них могут быть неразделимыми действующими веществами, что усложняет их индивидуальные исследования химических и физических свойств.
Универсальная индикаторная бумага
С развитием науки и появлением индикаторных бумаг установление показателей среды многократно упростилось, поскольку теперь не нужно было иметь готовые жидкие реактивы для каких-либо полевых исследований, чем до сих пор успешно пользуются ученые и криминалисты. Так, на смену растворам пришли универсальные индикаторные бумаги, которые благодаря широкому спектру действия практически полностью убрали необходимость использования любых других кислотно-основных индикаторов.
Состав пропитанных полосок может отличаться у различных производителей, поэтому примерный список входящих веществ может быть следующим:
- фенолфталеин (0-3,0 и 8,2-11);
- (ди)метиловый желтый (2,9-4,0);
- метиловый оранжевый (3,1-4,4);
- метиловый красный (4,2-6,2);
- бромтимоловый синий (6,0-7,8);
- α‒нафтолфталеин (7,3-8,7);
- тимоловый синий (8,0-9,6);
- крезолфталеин (8,2-9,8).
На упаковке обязательно приведены эталоны цветной шкалы, позволяющие определить pH среды от 0 до 12 (где-то 14) с точностью до одной целой.

Помимо прочего, данные соединения могут использоваться совместно в водных и водно-спиртовых растворах, что делает применение таких смесей очень удобным. Однако некоторые из этих веществ могут быть плохо растворимы в воде, поэтому необходимо подбирать универсальный органический растворитель.
Благодаря своим свойствам кислотно-основные индикаторы нашли свое применение во многих областях науки, а их многообразие позволило создать универсальные смеси, чувствительные к широкой области показателей pH.
При проведении химического процесса чрезвычайно важно бывает проследить за условиями протекания реакции или установить достижение ее окончания. Иногда это удается наблюдать по некоторым внешним признакам: прекращению выделения пузырьков газа, изменению окраски раствора, выпадению осадка или, наоборот, переходу в раствор одного из компонентов реакции и т. п. В большинстве же случаев для определения окончания реакции пользуются реактивами вспомогательного действия, так называемыми индикаторами, которые вводят обычно в анализируемый раствор в небольших количествах.
Индикаторами называются химические соединения, способные изменять окраску раствора в зависимости от условий среды, не влияя при этом непосредственно на испытуемый раствор и на направление реакции. Так, кислотно-щелочные индикаторы изменяют окраску в зависимости от pH среды; окислительно-восстановительные индикаторы - от потенциала среды; адсорбционные индикаторы - от степени адсорбции и т. д.
Особенно широко применяют индикаторы в аналитической практике для титриметрического анализа. Они служат также важнейшим инструментом для контроля технологических процессов в химической, металлургической, текстильной, пищевой и других отраслях промышленности. В сельском хозяйстве при помощи индикаторов проводят анализ и классификацию почв, устанавливают характер удобрений и необходимое количество их для внесения в почву.
Различают кислотно-щелочные, флуоресцентные, окислительновосстановительные, адсорбционные и хемилюминесцентные индикаторы.
КИСЛОТНО-ЩЕЛОЧНЫЕ (PH) ИНДИКАТОРЫ
Как известно из теории электролитической диссоциации, растворенные в воде химические соединения диссоциируют на положительно заряженные ионы - катионы и отрицательно заряженные - анионы. Вода также диссоциирует в очень малой степени на ионы водорода, заряженные положительно, и ионы гидроксила, заряженные отрицательно:
Концентрацию водородных ионов в растворе обозначают символом .
Если концентрация водородных и гидроксильных ионов в растворе одинакова, то такие растворы нейтральны и pH = 7. При концентрации водородных ионов, соответствующей pH от 7 до 0, раствор кислый, если же концентрация гидроксильных ионов больше (pH = от 7 до 14), раствор щелочной.
Для измерения значения pH пользуются различными методами. Качественно же реакцию раствора можно определить с помощью специальных индикаторов, меняющих свою окраску в зависимости от концентрации водородных ионов. Такими индикаторами являются кислотно-щелочные индикаторы, которые реагируют на изменение pH среды.
Кислотно-щелочные индикаторы в подавляющем большинстве являются красителями или другими органическими соединениями, молекулы которых претерпевают структурные изменения в зависимости от реакции среды. Ими пользуются в титриметрическом анализе при реакциях нейтрализации, а также для колориметрического определения pH.
| Индикатор | Интервал pH перехода окраски | Изменение окраски |
|---|---|---|
| Метиловый фиолетовый | 0,13-3,2 | Желтая - фиолетовая |
| Тимоловый синий | 1,2-2,8 | Красная - желтая |
| Тропеолин 00 | 1,4-3,2 | Красная - желтая |
| - Динитрофенол | 2,4-4,0 | Бесцветная - желтая |
| Метиловый оранжевый | 3,1-4,4 | Красная - желтая |
| Нафтиловый красный | 4,0-5,0 | Красная - оранжевая |
| Метиловый красный | 4,2-6,2 | Красная - желтая |
| Бромтимоловый синий | 6,0-7,6 | Желтая - синяя |
| Феноловый красный | 6,8-8,4 | Желтая - красная |
| Метакрезоловый пурпуровый | 7,4-9,0 | Желтая - фиолетовая |
| Тимоловый синий | 8,0-9,6 | Желтая - синяя |
| Фенолфталеин | 8,2-10,0 | Бесцветная - красная |
| Тимолфталеин | 9,4-10,6 | Бесцветная - синяя |
| Ализариновый желтый Р | 10,0-12,0 | Бледно-желтая - красно-оранжевая |
| Тропеолин 0 | 11,0-13,0 | Желтая - срзнжевая |
| Малахитовый зеленый | 11,6-13,6 | Зеленовато-голубая - бесцветная |
Если необходимо повысить точность измерения pH, то пользуются смешанными индикаторами. Для этого подбирают два индикатора с близкими интервалами pH перехода окраски, имеющими в этом интервале дополнительные цвета. При помощи такого смешанного индикатора можно проводить определения с точностью до 0,2 единицы pH.
Широко пользуются также универсальными индикаторами, способными многократно изменять окраску в широком диапазоне значений pH. Хотя точность определения такими индикаторами не превышает 1,0 единицы pH, зато они позволяют вести определения в широком интервале pH: от 1,0 до 10,0. Универсальные индикаторы обычно представляют собой комбинацию из четырех - семи двухцветных или одноцветных индикаторов с различными интервалами pH перехода окраски, составленную таким образом, чтобы при изменении pH среды происходило заметное изменение окраски.
Например, выпускаемый промышленностью универсальный индикатор РКС - смесь семи индикаторов: бромкрезолового пурпурового, бромкрезолового зеленого, метилового оранжевого, тро-пеолина 00, фенолфталеина, тимолового синего и бромтимолового синего.
Этот индикатор в зависимости от pH имеет следующую окраску: при pH = 1 - малиновую, pH = 2 - розовато-оранжевую, pH =3 - оранжевую, pH = 4 - желто-оранжевую, pH =5 желтую, pH = 6 - зеленовато-желтую, pH = 7 - желто-зеленую,. РН = 8 - зеленую, pH = 9 - сине-зеленую, pH = 10 - серовато-синюю.
Индивидуальные, смешанные и универсальные кислотно-щелочные индикаторы обычно растворяют в этиловом спирте и по нескольку капель добавляют в испытуемый раствор. По изменению окраски раствора судят о значении pH. Кроме спирторастворимых индикаторов, выпускаются также водорастворимые формы, представляющие собой аммонийные или натриевые соли этих индикаторов.
Во многих случаях удобнее пользоваться не растворами индикаторов, а индикаторными бумажками. Последние готовят следующим образом: фильтровальную бумагу пропускают через стандартный раствор индикатора, отжимают бумагу от избыточного раствора, высушивают, разрезают на узкие полоски и брошюруют в книжечки. Для проведения испытания индикаторную бумажку опускают в испытуемый раствор или одну каплю раствора помещают на полоску индикаторной бумажки и наблюдают изменение ее окраски.
ФЛУОРЕСЦЕНТНЫЕ ИНДИКАТОРЫ
Некоторые химические соединения при воздействии на них ультрафиолетовых лучей обладают способностью при определенном значении pH вызывать флуоресценцию раствора или изменять ее цвет или оттенок.
Этим свойством пользуются для кислотно-щелочного титрования масел, мутных и сильно окрашенных растворов, поскольку обычные индикаторы для этих целей непригодны.
Работу с флуоресцентными индикаторами проводят при освещении исследуемого раствора ультрафиолетовым светом.
| Индикатор | Интервал pH изменения флуоресценции (в ультрафиолетовом свете) | Изменение цвета флуоресценции |
| 4-Этоксиакридон | 1,4-3,2 | Зеленый - синий |
| 2-Нафтиламин | 2,8-4,4 | Нарастание фиолетовой флуоресценции |
| Диметнлнафтэйродин | 3,2-3,8 | Лиловый - оранжевый |
| 1-Нафтиламнн | 3,4-4,8 | Нарастание синей флуоресценции |
| Акридин | 4,8-6,6 | Зеленый - фиолетовый |
| 3,6-Диоксифталимид | 6,0-8,0 | Желто-зеленый - желтый |
| 2,3-Дициангидрохинон | 6,8-8,8 | Синий - зеленый |
| Эухризин | 8,4-10,4 | Оранжевый - зеленый |
| 1,5-Нафтиламинсульфамид | 9,5-13,0 | Желтый - зеленый |
| СС-кислота (1,8-аминонафтол 2,4-дисульфокислота) | 10,0-12,0 | Фиолетовый - зеленый |
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ИНДИКАТОРЫ
Окислительно-восстановительные индикаторы - химические соединения, изменяющие окраску раствора в зависимости от значения окислительно-восстановительного потенциала. Они применяются в титриметрических методах анализа, а также в биологических исследованиях для колориметрического определения окислительно-восстановительного потенциала.
| Индикатор | Нормальный окислительно-восстановительный потенциал (при рН=7), В | Окраска раствора | |
| окислительная форма | восстановленная форма | ||
| Нейтральный красный | -0,330 | Красно-фиолетовая | Бесцветная |
| Сафранин Т | -0,289 | Коричневая | Бесцветная |
| Индигомоносульфонат калия | -0,160 | Синяя | Бесцветная |
| Индигодисульфонат калия | -0,125 | Синяя | Бесцветная |
| Индиготрисульфонат калия | -0,081 | Синяя | Бесцветная |
| Инднготетрасульфонат калия | -0,046 | Синяя | Бесцветная |
| Толуидиновый голубой | +0,007 | Синяя | Бесцветная |
| Тнонин | +0,06 | Фиолетовая | Бесцветная |
| о-Крезолиндофенолят натрия | +0,195 | Красновато-синяя | Бесцветная |
| 2,6-Днхлорфенолиндофенолят натрия | +0,217 | Красновато-синяя | Бесцветная |
| м-Бромфенолиндофенолят натрия | +0,248 | Красновато-синяя | Бесцветная |
| Дифеинлбензидин | +0,76 (кислый раствор) | Фиолетовая | Бесцветная |
АДСОРБЦИОННЫЕ ИНДИКАТОРЫ
Адсорбционные индикаторы - вещества, в присутствии которых происходит изменение цвета осадка, образующегося при титровании методом осаждения. Изменять цвет осадка при определенном значении pH способны многие кислотно-щелочные индикаторы, некоторые красители и другие химические соединения, что делает их пригодными для использования в качестве адсорбционных индикаторов.
| Индикатор | Определяемый ион | Ион осадитель | Изменение окраски |
| Ализариновый красный С | Желтая - розово-красная | ||
| Бромфеноловый синий | Желтая - зеленая | ||
| Сиреневая - желтая | |||
| Фиолетовая - сине-зеленая | |||
| Дифенилкарбазид | , , | Бесцветная - фиолетовая | |
| Конго красный | , , | Красная - синяя | |
| Синяя - красная | |||
| Флуоресцеин | , | Желто-зеленая - розовая | |
| Эозин | , | Желто-красная - красно фиолетовая | |
| Эритрозин | Красно-желтая - темно красная |
ХЕМИЛЮМИНЕСЦЕНТНЫЕ ИНДИКАТОРЫ
К этой группе индикаторов относятся вещества, способные при определенных значениях pH высвечивать видимым светом. Хемилюминесцентными индикаторами удобно пользоваться при работе с темными жидкостями, поскольку в данном случае в конечной точке титрования возникает свечение.
ИНДИКАТОРЫ в химии (лат. indicator указатель) - вещества, изменяющие свой цвет в присутствии тех или иных химических соединений в исследуемой среде (в растворе, в воздухе, в клетках, в тканях), а также при изменении pH или окислительно-восстановительного потенциала среды; широко применяются в биохимических, клинических и санитарно-гигиенических лабораториях.
И. применяют для определения конца реакции (точки эквивалентности) при титровании, для колориметрического определения величин pH или окислительно-восстановительных потенциалов, для обнаружения различного рода веществ в тех или иных исследуемых объектах. Для всех этих целей И. применяют в виде водных или спиртовых р-ров или в виде индикаторных бумажек, представляющих собой полоски фильтровальной бумаги, пропитанные И.
В зависимости от назначения и механизма действия И. подразделяют на ряд групп.
Кислотно-основные индикаторы представляют собой сложные органические соединения, изменяющие окраску (двухцветные И.) или ее интенсивность (одноцветные И.) в зависимости от pH среды. Двухцветным И. является, напр., лакмоид: в щелочной среде он имеет синюю окраску, а в кислой - красную. Примером одноцветных И. может служить фенолфталеин, бесцветный в кислой среде и малиновый в щелочной.
По теории Оствальда (W. Ostwald) кислотно-основные И. представляют собой слабые органические к-ты или основания, недиссоциированные молекулы которых имеют в р-ре иную окраску, чем образуемые ими анионы и катионы. Фенолфталеин, напр., является слабой к-той, не диссоциированные молекулы к-рой бесцветны, а анионы окрашивают р-ры в малиновый цвет. В р-рах И., представляющие собой слабые к-ты, диссоциируют по уравнению
где НА - не диссоциированные молекулы И., H + - ионы водорода, а A - - анионы И.
Константа ионизации таких И. равна
Ka = [Н + ] [А - ]/[НА] (2)
(квадратными скобками обозначены молярные концентрации соответствующих частиц).
И., представляющие собой слабые основания, диссоциируют по уравнению

где ВОН - не диссоциированные молекулы И., В+ - катионы И., а OH- - гидроксильные ионы.
Константа диссоциации этих И. равна
Kb = / (4)
Из уравнений 2 и 4 следует, что чем больше величина константы диссоциации, тем в большей степени распадаются И. на ионы и тем, следовательно, при более высоких концентрациях ионов H + (в тех случаях, когда П.- слабая к-та) или ионов OH - (в тех случаях, когда И.- слабое основание) подавляется его диссоциация и происходит изменение окраски. Разные И. имеют различную величину Ka и Kb., поэтому они изменяют свою окраску при различных значениях pH среды. Тот интервал значений pH, в к-ром происходит изменение окраски данного И., называют зоной действия или интервалом перехода И. Интервал перехода И. обычно равен величине pK ± 1, где pK равен -lgК. Точкой перехода И. называют то значение pH, при к-ром визуально наиболее отчетливо воспринимается перемена окраски И. Точка перехода приблизительно равна величине рК данного И.
Кислотно-основные И. широко применяют при титровании к-т и щелочей, а также для колориметрического измерения величины pH биол, жидкостей, клеток, тканей и др.
Титрование к-т и щелочей должно быть закончено в момент достижения точки эквивалентности, т. е. в момент, когда к титруемому р-ру к-ты (щелочи) добавлен такой объем титранта, в к-ром содержится эквивалентное количество к-ты (щелочи). Для этого необходимо применять такой И., точка перехода к-рого равна величине pH титруемого р-ра в точке эквивалентности (см. Нейтрализации метод). В табл. перечислены И., наиболее употребляемые при титровании к-т и оснований.
Качественное определение кислотности и щелочности производят с помощью так наз. нейтральных И., точка перехода которых находится практически при pH 7,0. К ним относятся, напр., лакмус, имеющий в кислой среде (pH меньше 7,0) красный, а в щелочной среде (pH больше 7,0) синий цвет; нейтральный красный, окрашивающийся в кислой среде в красный цвет, а в щелочной - в желтый цвет.
Приближенное измерение величины pH среды (с точностью до 0,5- 1,0 ед. pH) обычно производят с помощью универсального (комбинированного) И., представляющего собой смесь нескольких И., интервалы перехода которых близки друг к другу и охватывают широкую область значений pH.
К 0,5 мл испытуемой жидкости добавляют 1-2 капли р-ра универсального И. и появляющуюся при этом окраску сравнивают с прилагаемой цветовой шкалой, на к-рой указаны значения pH, отвечающие различным окраскам И. Применяют также полоски фильтровальной бумаги, пропитанные универсальным И.
Для более точного (0,1-0,5 ед. pH) колориметрического определения величины pH обычно пользуются одноцветными И. ряда динитро- и нитрофенолов, предложенными Михаэлисом (L. Michaelis) и представляющими собой слабые к-ты, изменяющие окраску от бесцветной (в кислой среде) до желтой (в щелочной). С этой же целью пользуются рядом двухцветных И., предложенных Кларком (W. М. Clark) и Лабсом (H. A. Lubs), представляющих собой сульфофталеины. Кислотная и щелочная формы этих И. резко различаются по цвету, в этом состоит их преимущество по сравнению с индикаторами Михаэлиса.
Окислительно-восстановительные, или редоксиндикаторы , представляют собой органические красители, цвет которых в окисленном и восстановленном состоянии различен. Такие И. применяют при оксидиметрическом титровании (см. Оксидиметрия), а также для колориметрического определения величин окислительно-восстановительных потенциалов жидкостей (см. Окислительно-восстановительный потенциал), отдельных клеток и тканей в цитохим, и цитол, лабораториях. Большинство редокс-индикаторов при восстановлении превращается в бесцветные соединения, а при окислении окрашивается. Окисленная и восстановленная формы И. находятся в р-рах в состоянии динамического равновесия:
окисленная форма + ne <-> восстановленная форма, где n - число электронов.
Соотношение между равновесными концентрациями двух форм данного И., а следовательно, и цвет р-ра, в к-ром находится И., зависят от величины окислительно-восстановительного потенциала р-ра. Если величина потенциала р-ра больше нормального окислительно-восстановительного потенциала (Е0) данного редокс-индикатора, то большая часть И. в этом р-ре переходит в окисленную форму (обычно окрашенную), если же окислительно-восстановительный потенциал исследуемой среды меньше Е0, то И. превращается в восстановленную форму (обычно бесцветную). При равенстве значений окислительно-восстановительного потенциала среды и Е0 индикатора концентрации окисленной и восстановленной форм И. равны друг другу. Имея ряд И. с различными значениями Е0, можно по их окраске в данной среде судить о величине окислительно-восстановительного потенциала данной среды. Редокс-индикаторы, предложенные Михаэлисом, имеющие общее название «виологены» и представляющие собой производные гамма- и гамма"-дипиридилов, обладают малой токсичностью и широко применяются для измерения окислительно-восстановительных потенциалов в биол, системах; у этих И. окрашена восстановленная форма.
Нормальный окислительно-восстановительный потенциал виологенов не зависит от величины pH р-ра. Этим они отличаются от других редокс-индикаторов.
Комплексонометрические индикаторы (металлоиндикаторы) представляют собой хорошо растворимые в воде органические красители, способные образовывать с ионами металлов окрашенные комплексные соединения. Эти И. применяются для установления точки эквивалентности при комплексонометрическом титровании (см. Комплексонометрия).
Адсорбционные индикаторы - это органические красители, адсорбирующиеся на поверхности осадков, образующихся при титровании по методу осаждения, и изменяющие свой цвет при достижении точки эквивалентности. Напр., тропеолин 00 при титровании хлоридов р-ром азотнокислого серебра меняет окраску в точке эквивалентности с желтой на розовую.
Хемилюминесцентныe (флюоресцентные) индикаторы - органические соединения (например, люменол, люцегинин, силаксен и др.), обладающие способностью люминесцировать при естественном освещении или при облучении ультрафиолетовым светом. Интенсивность и цвет люминесценции зависят как от величины pH среды, так и от величины ее окислительно-восстановительного потенциала; эти И. применяются при титровании (при нейтрализации и оксидиметрии) сильно окрашенных или мутных жидкостей, когда изменение окраски обычных И. незаметно.
И. используются во многих биохим. методах, применяемых в клин.-биохим. лабораториях. Наиболее употребимыми из них являются бромтимоловый синий (при определении активности фруктозодифосфатальдолазы в сыворотке крови, активности ацетилхолинэстеразы и холинэстеразы в сыворотке крови по А. А. Покровскому, а также активности карбоксилэстеразы в крови по А. А. Покровскому и Л. Г. Пономаревой), бромфеноловый синий (при электрофоретическом разделении различных белков для окраски электрофореграмм наряду с амидочерным и кислотным сине-черным), универсальный И., феноловый красный (при определении активности аспартат- и аланин-аминотрансфераз в сыворотке крови, активности холинэстеразы в сыворотке крови и т. д.), фенолфталеин, нитросиний тетразолий, используемый для качественной и количественной оценки активности различных дегидрогеназ (см. Дегидрогеназы), и др.
|
Название индикатора |
Интервал перехода индикатора, в единицах pH |
||
|
Кислотная форма индикатора |
Щелочная форма индикатора |
||
|
Тропеолин 00 (дифениламиноазо-n-бензолсульфонат натрия) |
|||
|
Диметиловый желтый (диметиламиноазобензол) |
Оранжево-красный |
||
|
Метиловый оранжевый (диметиламиноазобензолсульфонат натрия) |
|||
|
Метиловый красный (диметиламиноазобензолкарбоновая к-та) |
|||
|
Феноловый красный (фенолсульфофталеин) |
|||
|
Фенолфталеин |
Бесцветный |
Малиновый |
|
|
Тимолфталеин |
Бесцветный |
||
Библиография: Виноградова E. Н. Методы определения концентрации водородных ионов, М., 1956, библиогр.; Индикаторы, под ред. Э. Бишопа и И. Н. Марова, пер. с англ., т. 1-2, М., 1976, библиогр.